pH(ペーハー)という言葉をご存知ですか?
日本語では【水素イオン濃度】といいいます。
多くの方が、小学生時代に理科の実験で、色々な液体にリトマス試験紙を浸して、紙の変化した色合いでpHを測定したことがあると思います。
そんなpHの違いや、水に与える影響などを調べてみました
pHとは?
まずは、pHというもの詳しく見ていきましょう
pHとは、その液体が酸性なのか、アルカリ性なのかを表す尺度となっております。
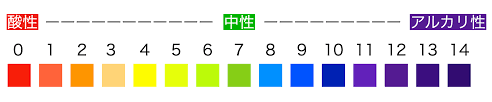
表し方としては1~14までの数値となり、真ん中の7が『中性』としてどちらでもない状態
値が7より低いと『酸性』、値が7より高いと『アルカリ性』と判断することができます。
『酸性』と『アルカリ性』は何が違うかと言うと、溶液中の水素イオン濃度が水酸化物イオン濃度よりも高い状態が『酸性』
水素イオン濃度と水酸化イオン濃度が等しい場合は、『中性』
水酸化物イオン濃度が水素イオン濃度より高い状態が『アルカリ性』となっております
酸性
酸性と聞いて、皆さんがイメージするのが物をドロドロに溶かす『硫酸』などかと思います。
しかし、酸性と言ってもpHの数値でいうと1~6まで存在し、強弱があります
酸性には鉄などの金属を溶かす性質をもちますが、強さによってことなります。
下の表のように、値が低い程、酸性の度合いが強いということになります
| 液性 | pHの範囲 |
|---|---|
| 酸性 | pH < 3.0 |
| 弱酸性 | 3.0 ≦ pH < 6.0 |
| 中性 | 6.0 ≦ pH ≦ 8.0 |
| 弱アルカリ性 | 8.0 < pH ≦ 11.0 |
| アルカリ性 | 11.0 < pH |
ちなみに身の回りの物で酸性の物は・・・
・醤油・・・pH5前後
・ビール・・・pH4.5前後
・ワイン・・・pH3.0前後
・コーラ・・・pH2.0前後
・食酢・・・pH2.0前後
人肌は一般的にはpH4.5~6.0前後の弱酸性と言われています。胃液中に含まれる胃酸はpH1.0~2.0ほどの強い酸性で食べ物を分解するだけでなく、微生物などを殺菌する作用もあるようです。
ちなみに『酸』と『酸性』とでは少し異なり、簡単に説明すると『酸』は水に溶かす前に対して、『酸性』は酸を水に溶かした状態
アルカリ性
酸性が鉄など金属を溶かす性質があるのに対して、アルカリ性はタンパク質などを溶かす性質があります。
酸性の水溶液は酸っぱく、触るとチクチクする感じだが、アルカリ性の水溶液は苦みがあり、触るとヌルヌルする感じがあります。(※触ったり、舐めたりすると非常に危険です!!)
アルカリ性の食品
・トマト
・ニンジン
・きゅうり
・レモン
・梅干し
etc
他のアルカリ性の物
・石鹸・・・pH10~11
・石灰水・・・pH11~12
・油汚れ用洗剤・・・pH12~13
洗剤は酸性の物や、アルカリ性の物があるかと思いますが、汚れが酸性の物に対して、アルカリ性の洗剤で中和させて落とす、汚れがアルカリ性の物も一緒の原理で使い分けましょう!
| 酸性の汚れ | ・油汚れ ・皮脂汚れ |
| アルカリ性の汚れ | ・水垢汚れ ・石鹸カス ・カルキ |
ちなみに中性洗剤は、酸性やアルカリ性と比べると洗浄力は劣りますが、手肌や素材を傷めることなく、軽い汚れを落とすために使用するという魅力があります。
水のpH
飲料水に最も適しているpH値は、中性~弱アルカリ性のpH7~8と言われています。
水道法の水質基準値としてはpH5.8以上~8.6以下が基本的な指標とされているようです
体内は中性~弱酸性に保たれていますので、飲料水が最も吸収されやすいpHは7~8と言えるでしょう
少しでも水道水が酸性に偏ってしますと酸味がある水になってしまい、アルカリ性に偏ってしまうと苦味やヌルヌルとした感覚があり、下痢になってしまう恐れがあります。
更に水道水のpHが変化すると水道管の腐食の原因となる可能性もあります。
自分たちで、pHを測定しろとまでは言いませんので、少しでも違和感を感じましたら、水道局へ連絡しましょう!
ちなみにpH測定用の試験紙は売っております。笑





コメント